チオエステルの有機合成反応
(1)ワンポットラクトン化反応
チオエステルは安定なアシル化剤として有機合成で汎用されています。しかし、その多くが塩基性条件であり、中性条件では反応が進行しません。金属触媒反応では正宗先生が量論量のCu(II), Hg(II)塩を用いたアシル化反応を報告されているにすぎず(JACS, 3575(1973))、中性条件下での触媒反応の報告例はありませんでした。
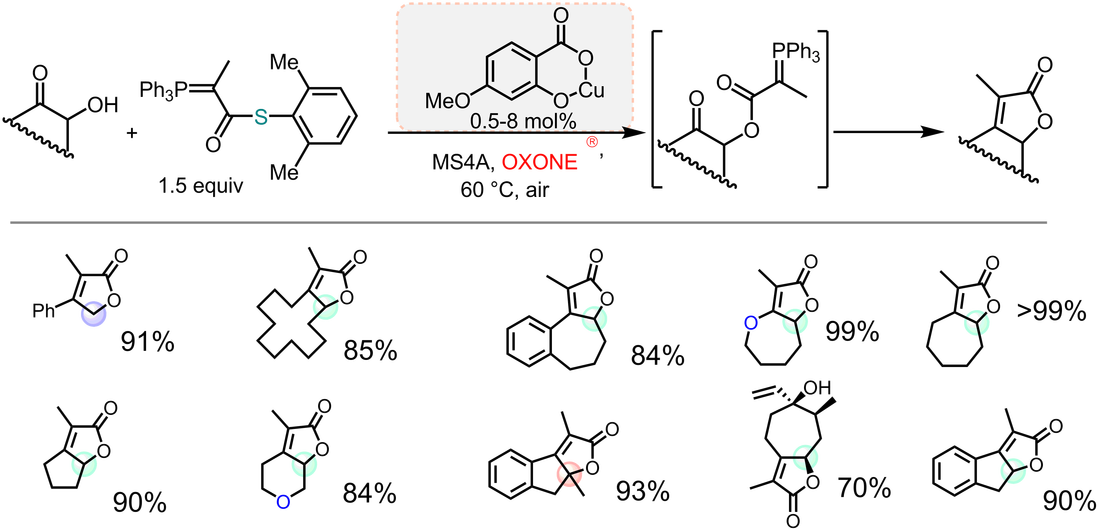
我々はsundiversifolideの全合成研究でチオエステルを組み込んだWittig反応剤を開発し、中性条件下でアシル化(エステル交換反応)に引き続くWittig反応でラクトンをワンポットで合成する反応を見出しました。また、銅(II)錯体を触媒にして共酸化剤(空気もしくはオキソン)を共存させることで反応の加速(よりマイルドな条件)に成功しました。すなわち中性触媒的アシル化反応の発見です。
ソフトルイス酸はチオエステルを活性化しますが、脱離したチオラートがその金属触媒を不活性化してしまうことが問題でした。我々は、チオラートを酸化してジスルフィドにすることで金属との相互作用を弱め、触媒化に成功しました。Org. Lett. 12, 5346(2010)
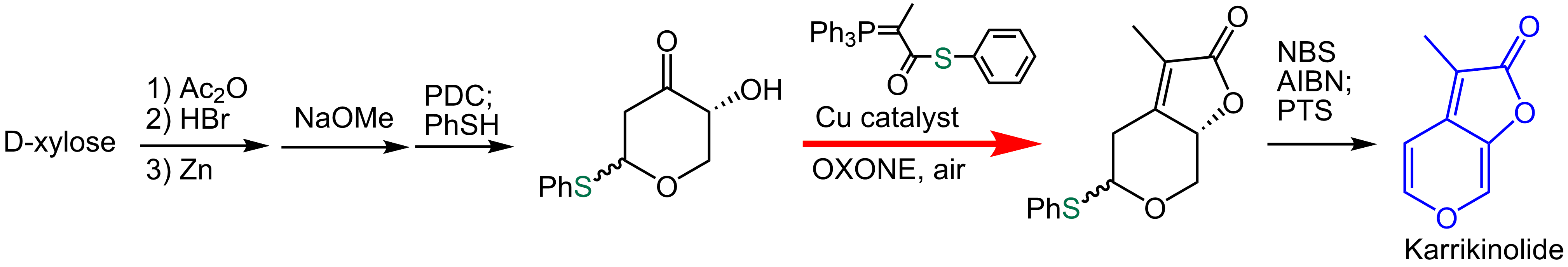
本反応を用いてキサンタノリド類の合成を達成しました。Tetrahderon 66, 8407(2010)
我々はsundiversifolideの全合成研究でチオエステルを組み込んだWittig反応剤を開発し、中性条件下でアシル化(エステル交換反応)に引き続くWittig反応でラクトンをワンポットで合成する反応を見出しました。また、銅(II)錯体を触媒にして共酸化剤(空気もしくはオキソン)を共存させることで反応の加速(よりマイルドな条件)に成功しました。すなわち中性触媒的アシル化反応の発見です。
ソフトルイス酸はチオエステルを活性化しますが、脱離したチオラートがその金属触媒を不活性化してしまうことが問題でした。我々は、チオラートを酸化してジスルフィドにすることで金属との相互作用を弱め、触媒化に成功しました。Org. Lett. 12, 5346(2010)
本反応を用いてキサンタノリド類の合成を達成しました。Tetrahderon 66, 8407(2010)
(2)マロン酸ジチオエステルの非対称化.
マロン酸エステルは有機合成で汎用される反応剤です。対称エステルは入手容易ですが、非対称エステルは意外に作りにくいものです。
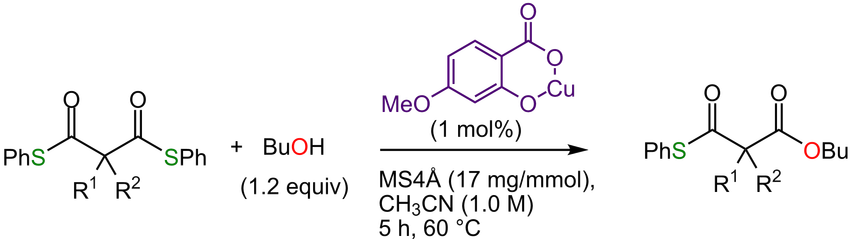
我々は、マロン酸のジチオエステルをアルコールと中性条件下で反応させるとモノエステルが高選択的に生成する非対称化反応を見出しました。ここに先ほどの銅触媒を加えますと、反応速度と選択性が格段に向上することも見出しました。Org. Lett. 13, 4406 (2011).
速度論研究から、中間体としてアシルケテンが生成していると考えています。
我々は、マロン酸のジチオエステルをアルコールと中性条件下で反応させるとモノエステルが高選択的に生成する非対称化反応を見出しました。ここに先ほどの銅触媒を加えますと、反応速度と選択性が格段に向上することも見出しました。Org. Lett. 13, 4406 (2011).
速度論研究から、中間体としてアシルケテンが生成していると考えています。