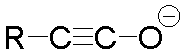イノラートの化学
カルバニオン(炭素陰イオン種)は基本的な反応活性種です。現代精密有機合成の花形は有機金属化学や遷移金属触媒化学であることは誰もが認めるところです。カルボアニオン種は有機合成の裏方として重要な役割を果たしていますが、これにちょっとした工夫を加えることで機能性反応種と化して精密有機合成の最先端に躍り出ることも可能なはずです。
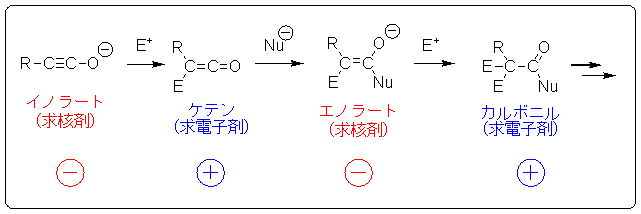
そこで我々が着目したのが「イノラート」と呼ばれるカルボアニオンです。これは教科書に出ている「エノラート」の二重結合を三重結合に変えただけの単純な化学種ですが、ケテンアニオン等価体でもあることから、エノラートとは比べ物にならないほどの機能性が期待できます。一例をお示しすると、下の図にありますようにイノラートは強い求核剤ですから求電子剤(E)と反応してケテンを与えます。ケテンは強い求電子剤ですから求核剤(Nu)と容易に反応します。そこで生じるのがご存じのエノラートです。従って求電子剤と反応してカルボニルを与える・・このようにイノラートは分子極性を転換させながら結合を形成し新たな反応活性種を生み出していくのです。我々はこれを極性転換型マルチ反応プロセスと呼んでいます。一つのフラスコの中で一挙に4工程も5工程も進行すればこれはまさに効率的合成、流行の言葉で言えば低環境負荷型反応なのです。しかしイノラートはその合成の難しさ、煩雑さからこれまでほとんど研究はなされていませんでした。
我々はイノラートの新規簡便合成法の開発に成功し、これを契機に次々と新反応を見出してきました。しかしこれらの成果はイノラートの化学の本の氷山の一角に過ぎないと考えています。イノラートは宝の山なのです。我々はさらにこれを有機合成に積極的に活用しようと考えています。
そこで我々が着目したのが「イノラート」と呼ばれるカルボアニオンです。これは教科書に出ている「エノラート」の二重結合を三重結合に変えただけの単純な化学種ですが、ケテンアニオン等価体でもあることから、エノラートとは比べ物にならないほどの機能性が期待できます。一例をお示しすると、下の図にありますようにイノラートは強い求核剤ですから求電子剤(E)と反応してケテンを与えます。ケテンは強い求電子剤ですから求核剤(Nu)と容易に反応します。そこで生じるのがご存じのエノラートです。従って求電子剤と反応してカルボニルを与える・・このようにイノラートは分子極性を転換させながら結合を形成し新たな反応活性種を生み出していくのです。我々はこれを極性転換型マルチ反応プロセスと呼んでいます。一つのフラスコの中で一挙に4工程も5工程も進行すればこれはまさに効率的合成、流行の言葉で言えば低環境負荷型反応なのです。しかしイノラートはその合成の難しさ、煩雑さからこれまでほとんど研究はなされていませんでした。
我々はイノラートの新規簡便合成法の開発に成功し、これを契機に次々と新反応を見出してきました。しかしこれらの成果はイノラートの化学の本の氷山の一角に過ぎないと考えています。イノラートは宝の山なのです。我々はさらにこれを有機合成に積極的に活用しようと考えています。
(1)イノラートの新規合成法
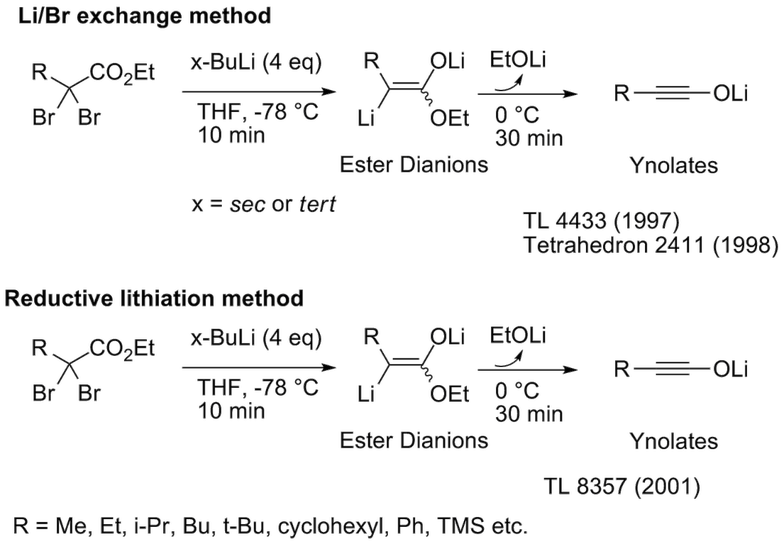
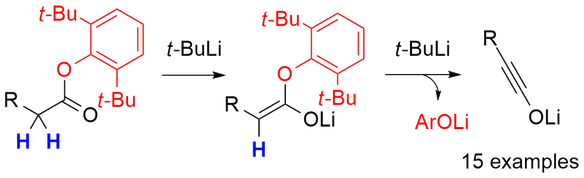
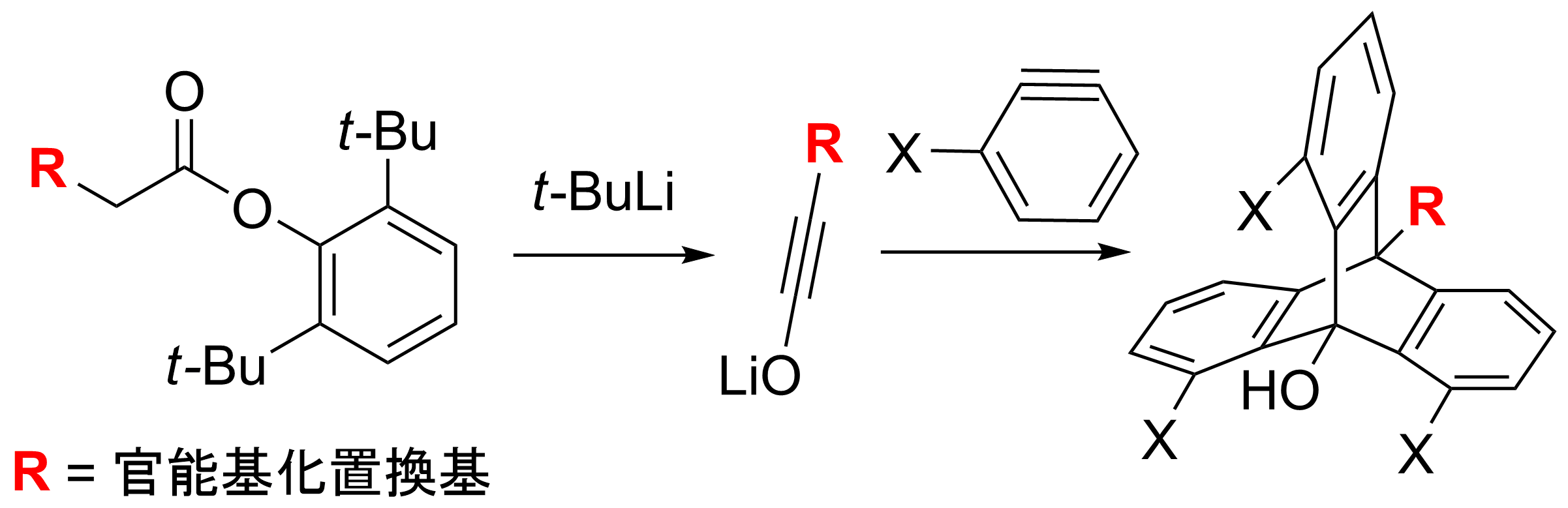
こんな魅力的なイノラートの研究がこれまで遅れていたのは、何と言ってもその合成の難しさにあります。我々はエステルジアニオンの熱開裂という新規概念によるイノラートの簡便な合成法の開発に成功しました。本手法は操作も簡便で配属直後の大学院生でも1、2回の練習ですぐにできるようになります。この方法の開発がイノラートの研究の起爆剤となりました。マイクロリアクターを用いた実用的合成法も開発しました。また、最近、非臭素化単純エステルからのイノラート生成法も見出しました(Org. Lett. のEditor's Choiceに選定され、Cover Figureを飾りました)。
Simple preparationof ynolates (OL 21, 6585, 2019【Editor's Choice】)
マイクロリアクターを用いたプロセス化学
錬金術の時代から数百年、有機反応といえばフラスコと決まっていました。しかしフラスコの中の反応は膨大な数の分子と分子の衝突の途方もない組み合わせの結果であり、決して反応式で表したような単純系ではありません。だからこそ収率が悪い、副生成物が出てくる、反応が暴走する、低温で・・などと思った通りにはいかないのではないでしょうか。理想的には分子の1対1の反応です。その理想に少しでも近づけるために、マイクロリアクターを初めとするフローデバイスに我々は注目しています。フロー系の反応、すなわち細管中での流れ場の反応は分子の自由度が著しく制限され、少なくともバッチ系よりは理想に近づいています(といっても道のりは長いのですが)。これまで厳密な低温制御が必要であった反応が室温できれいに進むことも我々は見いだしています。実用面でも大きなメリットがあります。連続的に流しておけばいくらでも大量合成ができます。大きな釜は不要です。実験室からそのまま工業プロセスへとスケールアップすることも可能でしょう。(北海道大学、名古屋大学との共同研究)
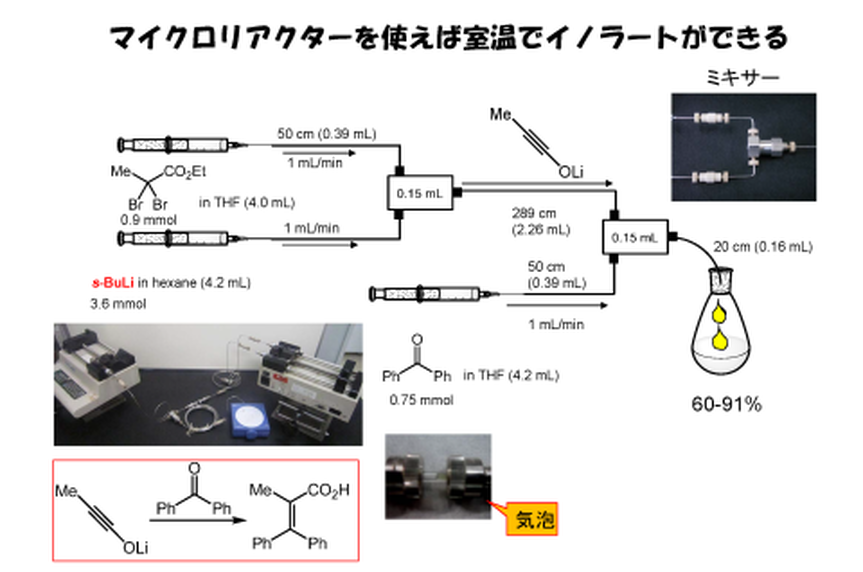
我々はマイクロリアクターでイノラートを生成することに成功しました。初めは機器の選択から試行錯誤でした。本来のマイクロリアクター(内径が数百マイクロメートル)ではどうしても途中で詰まってしまってNGでしたが、内径1mmぐらいのステンレスチューブでうまくいくようになりました。マイクロリアクターというよりミリリアクターですが・・・・。ミキサーも数十万円もする高価なものでは詰まってしまったら泣くに泣けないので、HPLC用の汎用品を使ってみました。結局、下の写真にあるような手作り?装置でブチルリチウムとジブロモエステルの溶液を混ぜて、1分ぐらい流したのちに反応剤と混ぜるというシステムにしました。条件検討の結果、イノラートを生成する際に室温でできるようになりました。フラスコの中では必ず-78度に冷却しなければいけなかったのが、室温で流すだけ!大量合成の時にたくさんのドライアイスを用意する必要がないのです。
T. Yoshiiwa, S. Umezu, M. Tokeshi, Y. Baba, M. Shindo, J. Flow Chem. 4, 180-184 (2014)
T. Yoshiiwa, S. Umezu, M. Tokeshi, Y. Baba, M. Shindo, J. Flow Chem. 4, 180-184 (2014)
しかし、収率がばらついて安定しませんでした。ステンレスチューブにのぞき窓(北大工。渡慶次教授特製)でよく調べてみると気泡が発生していることに気が付きました。ブチルリチウム由来のブタンガスやTHF由来のエチレンガスやら、低温では溶けていた期待が室温でガス化してしまいました。また、数分流すと、結局詰まってしまうこともしばしば。
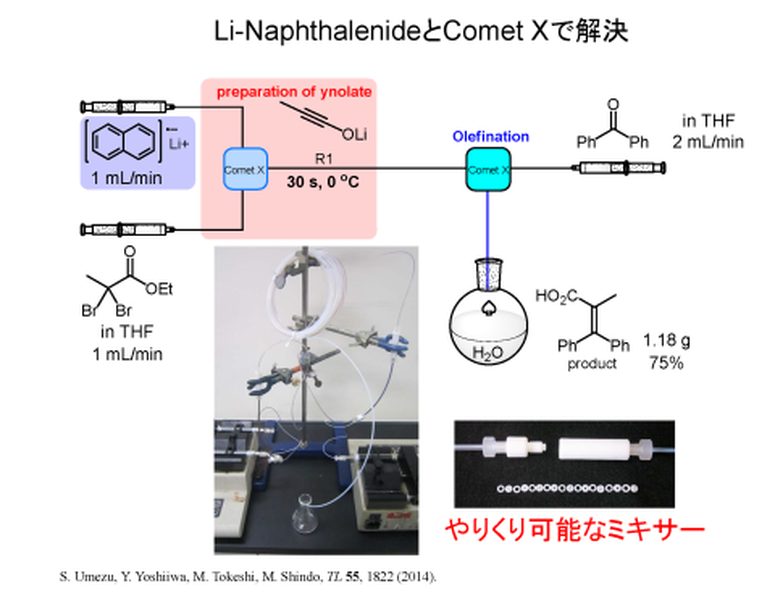
そこで出会ったのがCometX(テクノアプリケーションズ社製)でした。テフロン性のミキサーですが、内部構造を自由に変えられるので、少し緩めにしておけば多少ミキシング効率は落ちても詰まらなくなりました。そして、リチオ化法をブチルリチウムからリチウムナフタレニドによる還元的リチオ化に変えてみました。そうすると、ガスも発生せず、詰まることもなく、0度から室温で連続的にイノラートを生成できるようになりました。実際にグラムスケールの実験にも成功しています。原理的には、連続運転で何ぼでもできるはず・・・
そこで出会ったのがCometX(テクノアプリケーションズ社製)でした。テフロン性のミキサーですが、内部構造を自由に変えられるので、少し緩めにしておけば多少ミキシング効率は落ちても詰まらなくなりました。そして、リチオ化法をブチルリチウムからリチウムナフタレニドによる還元的リチオ化に変えてみました。そうすると、ガスも発生せず、詰まることもなく、0度から室温で連続的にイノラートを生成できるようになりました。実際にグラムスケールの実験にも成功しています。原理的には、連続運転で何ぼでもできるはず・・・
マイクロリアクターはフラスコ反応で困ったときや、大量合成のときに大きなフラスコを用意できないときなど、これからも有機合成で活躍しそうな気がします。
(2)イノラートの特性を生かした連続反応
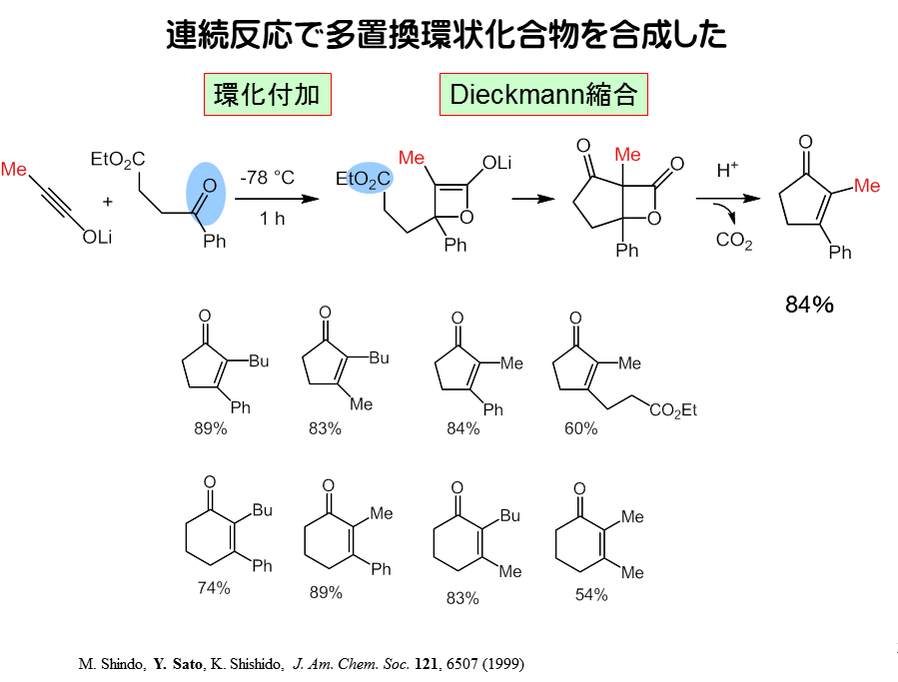
極性転換型マルチ反応プロセス第一号が [n+1] 型連続的環化反応です。イノラートとケトエステルを反応させると、まず、ケトンと反応してβーラクトンエノラートが生成し、これが速やかに Dieckmann 反応により閉環し縮合ラクトンが生成します。これを酸処理することで脱炭酸させると多置換シクロアルケノンが高収率で生成することを見出しました。この反応は種々の応用が可能で5,6,7員環や多置換ナフタレンも合成できます。多置換複素環のワンポット合成もできます。
本反応を利用した生物活性天然物の全合成も報告しています。(この連続反応は日本やアメリカの大学院生向けの問題集や試験問題に採用されています)。
本反応を利用した生物活性天然物の全合成も報告しています。(この連続反応は日本やアメリカの大学院生向けの問題集や試験問題に採用されています)。
ここをクリックして編集する.
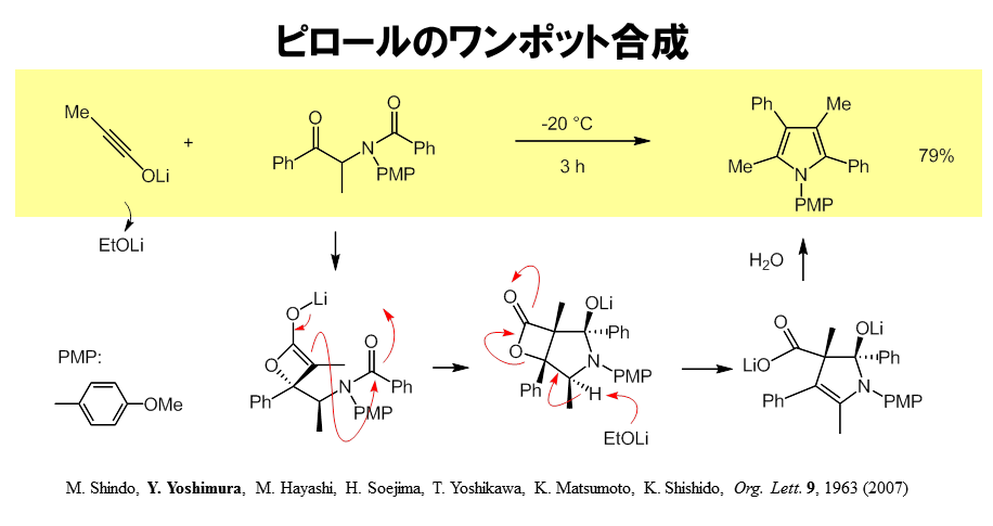
多置換複素環のワンポット合成
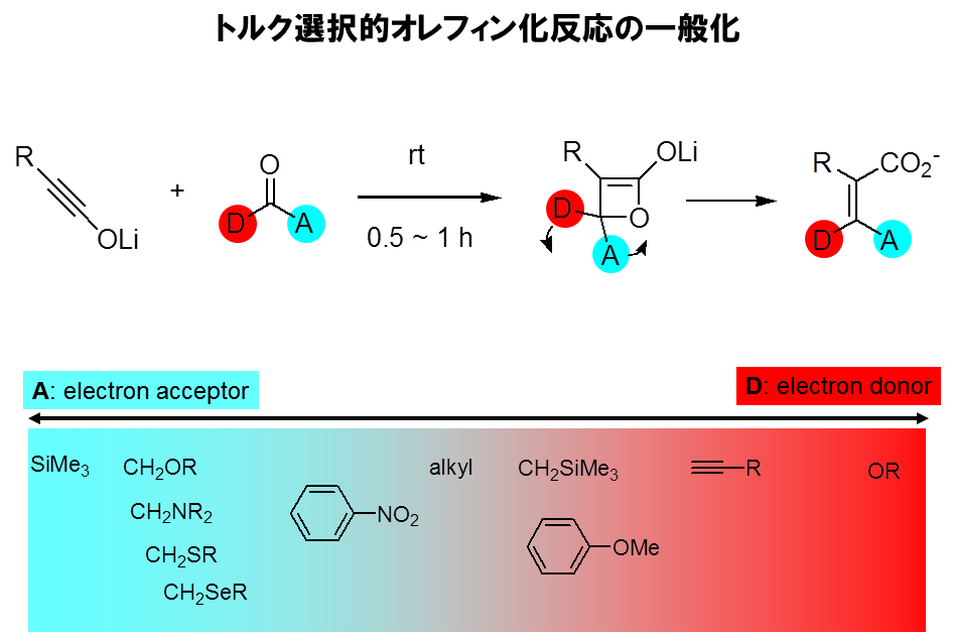
(3)回転選択的オレフィン化反応(Torquoselective olefination)
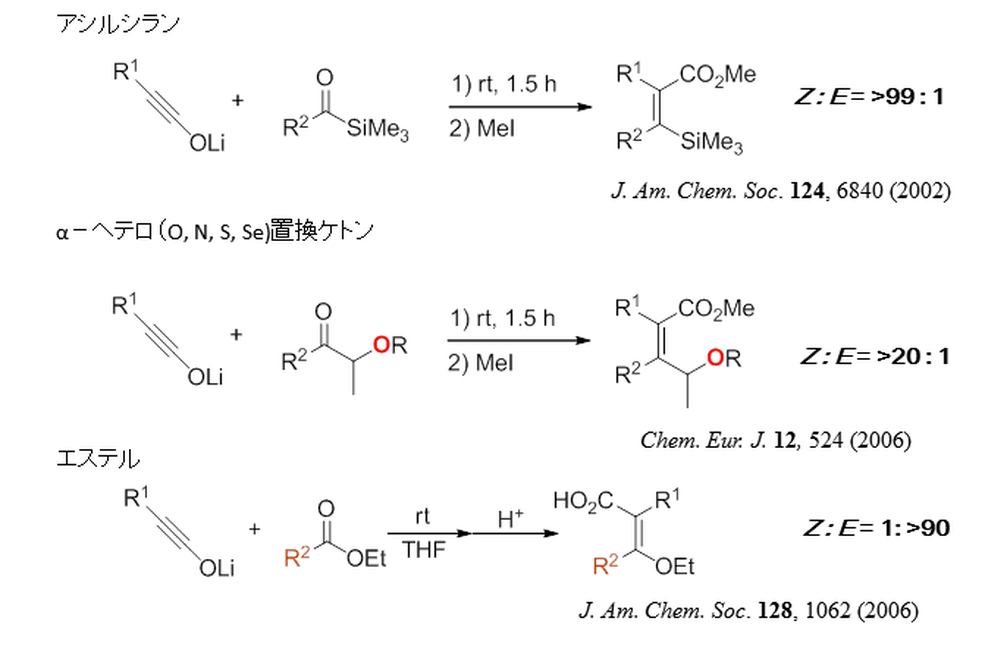
イノラートとカルボニルとの付加環化反応を室温付近で行うと中間体のβーラクトンエノラートが速やかに開環しオレフィンを与えることを見いだしました。このときのオレフィンの幾何異性は開環の際の回転の方向性(torquoselectivity)で決定づけられます。我々は様々なカルボニルのオレフィン化反応を試みたところ、アシルシラン、αーオキシケトン、αーアミノケトンなどを基質とすると極めて高い幾何選択性で四置換オレフィンが生成することを見いだしました。これはケトンのオレフィン化で高選択性を発揮した初めての成功例です。通常のオレフィン化反応では特に困難とされるエステルの高選択的オレフィン化反応にも成功しました。これらのオレフィン化反応は軌道相互作用によりtoruquoselectivityが制御されており、理論化学計算によってもそれは証明されております。それによるとカルボニルの置換基の電子的特性で説明され、電子供与性置換基がoutward、電子吸引性置換基がinwardに回転して選択性が発現します。オレフィン化反応の幾何選択性を理論的に予想することも可能です。また、立体障害に強く、込み入った多置換オレフィンの合成に威力を発揮します。我々はこれを"torquoselective olefination"と名付け、従来のイリド法(Wittig反応など)やカルベノイド法(Tebbe試薬など)に次ぐ第三のオレフィン化反応と位置づけています。今度、さらに発展することが期待されています。
総説: Synlett 2231 (2008): 有機合成化学協会誌, 66 (1) 28 (2008).Top. Curr. Chem. 327, 1 (2012).
総説: Synlett 2231 (2008): 有機合成化学協会誌, 66 (1) 28 (2008).Top. Curr. Chem. 327, 1 (2012).
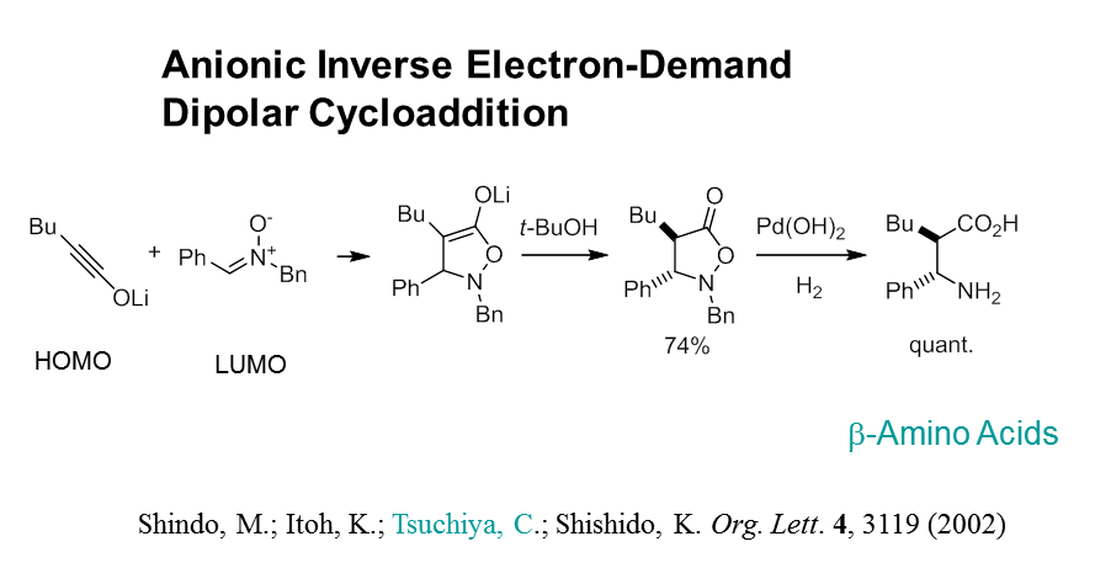
(4)逆電子要請型双極子環化付加反応
イノラートはニトロンと双極子環化付加型反応により5-isoxazolidinoneを好収率で与えることを見いだしました。この生成物は還元により容易にβ-アミノ酸へ導くことができます。当たり前の反応のように見えますが、ニトロンを基質にする双極子環化付加は通常、ニトロンがHOMOで相手がLUMOの反応例が圧倒的に多く、この例のようにイノラートがHOMOでニトロンがLUMOで考えるタイプの反応は少ないのです。兄弟アニオンのエノラートでは収率、立体選択性ともによい結果を与えないことから、この反応もイノラートの特性が生かされています。今後、β-アミノ酸などの含窒素有機化合物の合成に活用されるでしょう。
(5)超原子価化合物の創製と反応
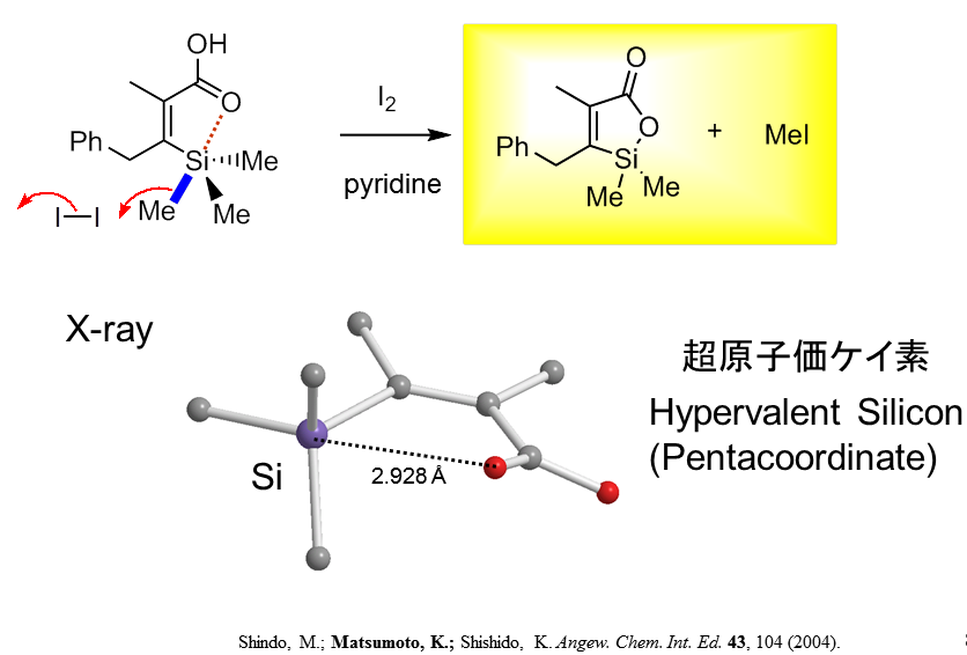
イノラートとアシルシランで生成したβ―シリルアクリル酸(エステル)をヨウ素と反応させてケイ素ーヨウ素交換反応を行おうとしたところ、意外にもシララクトンとヨウ化メチルが定量的に生成しました。本来安定なはずのケイ素―炭素結合が切断されている!!!!この現象に驚いた我々は様々な分析機器を駆使してその機構を調べたところ、カルボニルがケイ素に分子内高配位したためにそのケイ素が超原子価状態になっていたことが原因と判明しました。
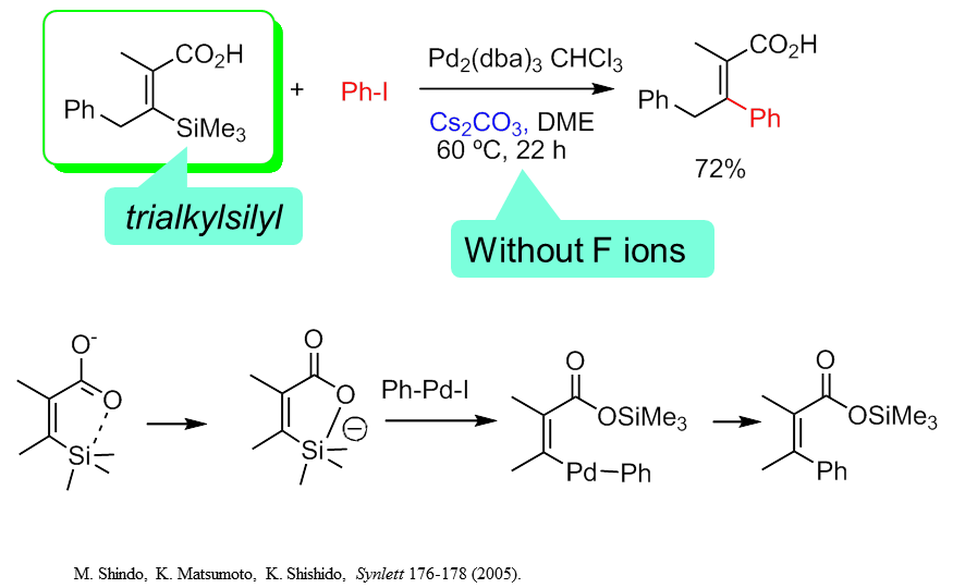
ケイ素の超原子価状態は決して珍しい現象ではありませんが、「分子内高配位により有機ケイ素化合物を活性化し合成反応へと展開する」研究は意外に少ないことに我々は着眼しました。例えば、ビニルシランとハロゲン化アリルとのカップリング反応(いわゆる檜山反応)は、その反応活性化に工夫が必要で、今なお活発に研究が進められています。我々は上記現象を利用すれば、フッ素イオンが存在しない緩和な条件下で檜山反応が容易に起こることを見出しました。
このカップリング反応はほんの一例です。有機ケイ素化合物に限った反応でもありません。これからもアイデア次第で多くの有用な新規反応が見出されると考えています
(6)新ナザロフ反応
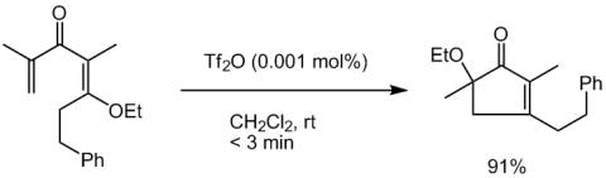
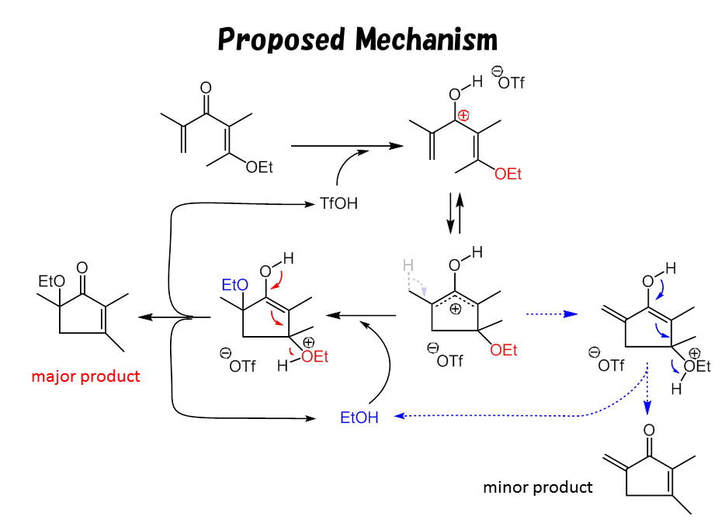
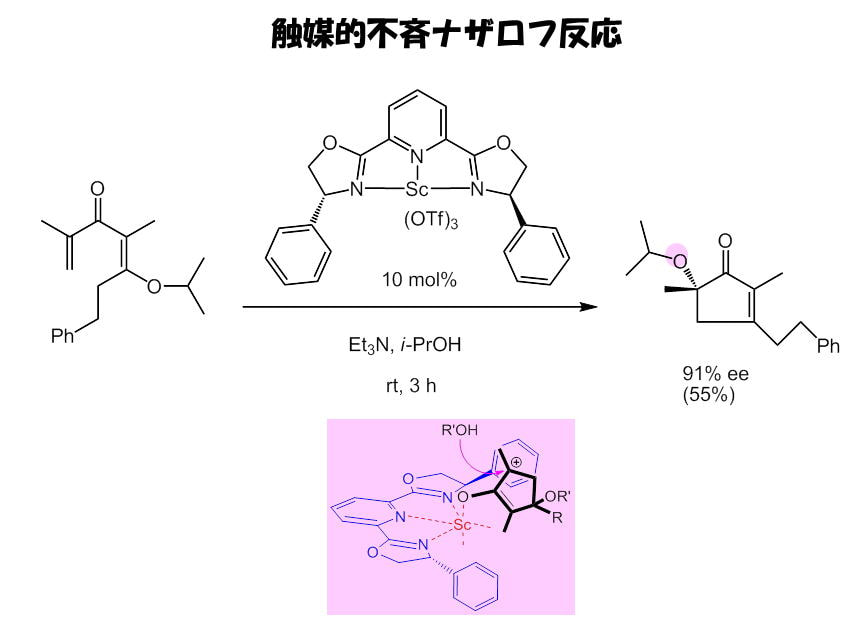
ナザロフ反応は古典的な電子環状反応ですが、強酸性条件下での加熱を要し近年まで合成反応としては制限が多い反応でした。この10年触媒的ナザロフ反応が報告されるようになり、現代精密有機合成化学の仲間入りをしました。我々はイノラートによるエステルのオレフィン化から着想を得て、新しい触媒的高速ナザロフ反応を開発しました。エステルのオレフィン化で得たβ―アルコキシアクリル酸をβ―アルコキシジビニルケトンへと誘導し、これを原料にごく微量のTfOHやルイス酸を加えるだけで室温でほぼ瞬時に反応が完結し、αーアルコキシシクロペンテノンが高収率で得られることを見出しました。アルコキシル基が見かけ上転位した新タイプのナザロフ反応です。不斉反応(最高91%ee)や天然物の全合成にも成功しました。
最近、さらにほぼ中性でも進行するナザロフ反応を見つけました。こうご期待!
Synlett 1096 (2007); Synlett 2524 (2009); TL 5469 (2010); Tetrahedron 9808 (2010)
最近、さらにほぼ中性でも進行するナザロフ反応を見つけました。こうご期待!
Synlett 1096 (2007); Synlett 2524 (2009); TL 5469 (2010); Tetrahedron 9808 (2010)
(7)イノラートを利用した天然有機化合物の合成
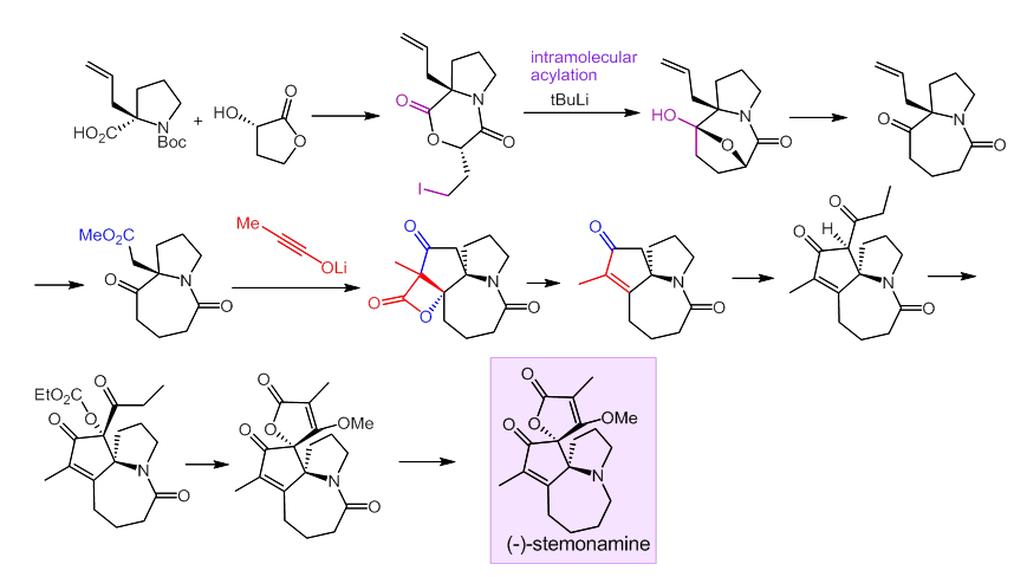
ステモナミンの全合成(初の光学活性体の全合成に成功!!!)
ステモナミンとイソステモナミンの不斉全合成に世界で初めて成功しました。置換基で埋め尽くされた立体的に込み入ったシクロペンタノンの合成に効果的にイノラートが働きました。
このアルカロイドはラセミ体として抽出されましたので、光学活性体を世界で初めて手にしたことになります。ステモナミンの立体化学的安定性も明らかにしました。
このアルカロイドはラセミ体として抽出されましたので、光学活性体を世界で初めて手にしたことになります。ステモナミンの立体化学的安定性も明らかにしました。